| Fyzikální vlastnosti |
| Vlastnosti |
Růst krystalů
Český název minerálu – nerost, vytvořil obrozenec J. S. Presl. Název nerost není příliš přesný, protože krystaly nerostů rostou. Rostou však samozřejmě jinak než živé organismy. Vznik nerostů probíhá ve dvou etapách. Nejdříve se seskupí nepatrné množství stavebních částic a vytvoří tak zárodek krystalu. Krystal pak roste připojováním dalších částic na povrch zárodku. Postupně se přikládají další a další částice. To znamená, že centrální část krystalu je nejstarší, zatímco jeho povrchová vrstva je nejmladší.
Částice, které se připojily k povrchu krystalu v krátkém časovém úseku, tvoří v krystalu určitou zónu. V průběhu krystalizace se mění řada fyzikálních a chemických podmínek, proto se od sebe jednotlivé zóny jednoho minerálu mohou lišit. Velmi výrazné zonální zbarvení mívají krystaly turmalínu.
Krystal roste v různých směrech různou rychlostí. Proto mohou vzniknout různé tvary, které u krystalů pozorujeme. Pokud by krystal rostl ve všech směrech stejně rychle, vznikla by koule. Velikost krystalu není teoreticky nijak omezena. V přírodě záleží na velikosti prostoru, ve kterém minerál krystaluje a také na množství matečného roztoku. Největší krystaly nalezené v přírodě dosahují velikosti několika metrů (výjimečně i více než 10 metrů) a hmotnosti několika tun (př. krystaly muskovitu a živce v pegmatitech).
| Fyzikální vlastnosti |
Tvrdost je odpor minerálu proti vniknutí cizího tělesa. Závisí na pevnosti vazby mezi částicemi v krystalové struktuře nerostu. Čím je vzdálenost částic menší, tím je vazba zpravidla pevnější a nerost tvrdší. Vazby mezi vzdálenějšími částicemi jsou slabší, a proto je nerost měkčí.
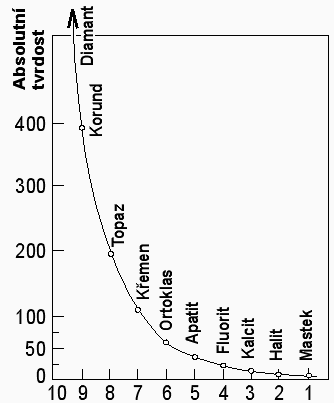
Mohsova stupnice tvrdosti:
Pro srovnání tvrdosti nerostů sestavil Friedrich Mohs (1773 - 1839) desetičlennou stupnici, seřazenou tak, že každý tvrdší nerost rýpe do předcházejícího měkčího. Například minerál s tvrdostí 4 rýpe do kalcitu (tvrdost 3), ale do apatitu (tvrdost 5) nerýpe. Tvrdost neoznačujeme jednotkami. Rozdíly tvrdosti mezi jednotlivými stupni jsou různé. Největší rozdíl je mezi 9. a 10. stupněm.
|
 |
Hustota určuje, kolikrát je určitý objem nerostu těžší než stejný objem destilované vody. Z fyziky víme, že se hustota udává v jednotkách g/cm3. Přibližně ji můžeme porovnat potěžkáním v ruce. Můžeme tak rozlišit minerály podobné velikostí a barvou (například živec od těžšího barytu). U většiny minerálů se hustota pohybuje v rozmezí hodnot 2 až 4 g/cm3. Velkou hustotu má zlato (19 g/cm3). To znamená, že krychle zlata o hraně 1 cm váží 19 gramů. Lépe si možná představíme krychli o hraně 10 cm, která by celá ze zlata vážila 19 kg.
Rozdílnost hustoty umožňuje oddělovat od sebe těžší nerosty od lehčích, například plavením nebo rýžováním. Těžší minerály (zlato, granáty) klesají na dno zlatokopecké pánve, zatímco lehké minerály se odplavují a při krouživém pohybu vypadávají z pánve ven.
Po úderu kladivem do minerálu můžeme pozorovat, jak se minerál rozpadá. Vidíme štěpnost nebo lom. Ve většině případů však není nutné vzorek poškodit, stačí pozorovat jeho plochy. Minerály se štípou na úlomky podle rovných lesklých štěpných ploch ve směrech, kde je nejmenší soudržnost. Počet směrů (rovin) štěpnosti může být u různých minerálů různý. V jednom směru jsou štěpné slídy a tuha, ve dvou směrech amfibol, ve třech směrech galenit (rozpadá se na krychle) a kalcit (rozpadá se na klence), ve čtyřech směrech fluorit (rozpadá se na osmistěn), v šesti směrech sfalerit.
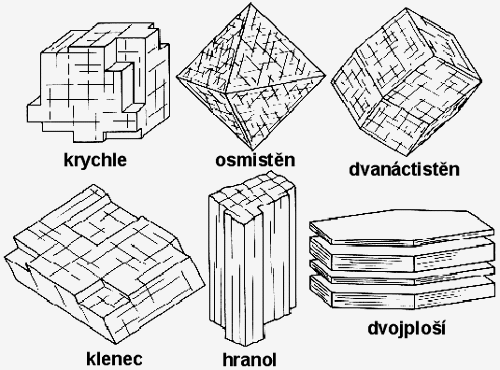
Některé nerosty se lámou podle nerovných ploch. Lomné plochy nejsou závislé na struktuře.
Podle vzhledu lomné plochy rozeznáváme například: nerovný lom, miskovitý, hladký, tříšťnatý a lasturnatý lom (křemen, opál, obsidián).
Kujné minerály
Některé minerály jsou kujné. Patří mezi ně většina ryzích kovů - zlato, stříbro, měď. Nerozpadají se, nýbrž je lze rozklepat do tenkých plíšků. Velmi tenké zlaté fólie nazelenale prosvítají.
Lesk vzniká odrazem světla od krystalových nebo štěpných ploch. Rozlišujeme například:
Barva je jednou z nejnápadnějších vlastností minerálů. Je důležitá pro poznávání minerálů. Rozlišujeme nerosty barevné, bezbarvé a zbarvené. U barevných nerostů je barva velmi stálá. Magnetit je vždy černý, malachit zelený, azurit modrý... Stejnou barvu jako minerál mívá obvykle i jeho vryp. (Výjimku tvoří např. mosazně žlutý chalkopyrit, který má tmavě šedý vryp). Jako bezbarvé nerosty označujeme ty, které jsou čiré a mají bílý vryp. Zbarvené nerosty jsou zbarveny díky různým příměsím, ale jejich vryp zůstává bílý, šedý nebo jen slabě zabarvený.
Mnohobarevnost (pleochroismus)
Mnohobarevnost můžeme okem pozorovat jen u některých minerálů. Jejich krystaly při natáčení mění barvu (např. turmalín, rubín, safír). Nejlépe lze tuto vlastnost v polarizačním mikroskopu.
Podle propustnosti světla rozlišujeme nerosty průhledné, průsvitné a neprůsvitné.
Vryp je barva prášku, kterou zanechává nerost při otírání o neglazovanou bílou porcelánovou destičku. Může se lišit od skutečné barvy nerostu.
Některé minerály odolávají vysokým teplotám. Příkladem může být muskovit (světlá slída). Používá se jako izolační materiál. Vyrábí se z něho žáruvzdorná okénka („americká" kamna). Dalším příkladem je grafit (tuha) - má bod tání 2800°C.
Dobrými vodiči elektrického proudu jsou kovy (měď, stříbro, zlato) a grafit.
Nevodivé jsou například jílové minerály a karbonáty.
Nejhojnějším a nejznámějším ferromagnetickým minerálem je magnetit.
| Chemické vlastnosti |
Minerály se skládají z malých částic - atomů iontů a molekul. Chemické složení minerálů se vyjadřuje chemickou značkou (síra - S) nebo chemickým vzorcem (galenit - PbS).
Minerály se rozdělují podle chemického složení a vnitřní stavby do devíti tříd mineralogického systému.
Polymorfní nerosty mají stejné chemické složení, ale vznikly za různých podmínek. Mohou proto krystalovat v různých soustavách.
Příklady: C: diamant - grafit, CaCO3: kalcit - aragonit, FeS2: pyrit - markazit.
Izomorfní minerály mají různé složení, ale stejné (nebo velmi podobné) vlastnosti. Izomorfní minerály tvoří přirozené řady, např. uhličitany kalcitové řady: kalcit CaCO3 - magnezit MgCO3 - siderit FeCO3. Stavební částice izomorfních minerálů se mohou ve struktuře navzájem zastupovat, proto se v přírodě často setkáváme s kalcitem, který obsahuje také hořčík (tzv. hořečnatý kalcit).
Nejčastěji se používá reakce se zředěnou kyselinou chlorovodíkovou (HCl) k důkazu uhličitanů. Při této reakci se uvolňují bubliny CO2 (šumění). Tato reakce probíhá u některých uhličitanů za studena (kalcit, aragonit), u jiných je třeba úlomek minerálu v kyselině zahřát (ve zkumavce). K důkazu karbonátů, které reagují s HCl za studena, můžeme použít místo HCl běžný kuchyňský ocet.
Zlato se rozpouští v lučavce královské, což je směs kyseliny dusičné (HNO3) a kyseliny chlorovodíkové (HCl).
Ve vodě je rozpustný halit (sůl kamenná, NaCl).
Řada prvků význačně barví plamen. U některých nerostů dochází k barvení plamene již při vsunutí vzorku do plamene, jiné musíme nejprve ovlhčit kyselinou. Většinou používáme zředěnou kyselinu chlorovodíkovou.
| Zbarvení | Odstín | Prvek | Symbol |
| červené | cihlový | vápník | Ca |
| purpurový | lithium | Li | |
| karmínový | stroncium | Sr | |
| žluté | žlutý | sodík | Na |
| zelené | světle žlutozelený | baryum | Ba |
| zelený | měď | Cu | |
| velmi slabě zelený | antimon | Sb | |
| modré | šedomodrý | arsen | As |
| fialové | bleděfialový | draslík | K |
| šedofialový | rtuť | Hg |