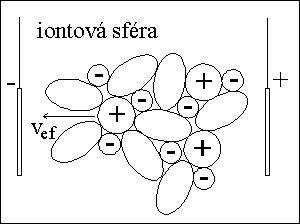
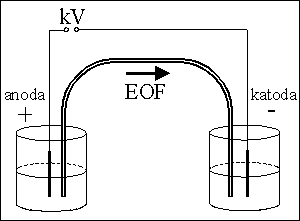
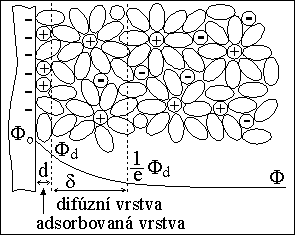
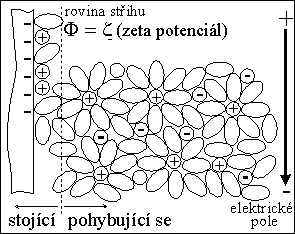
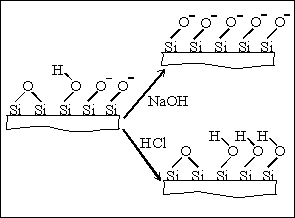
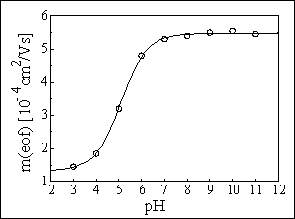
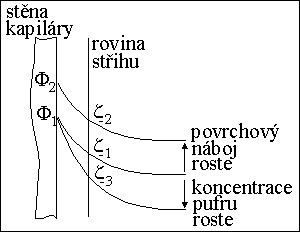
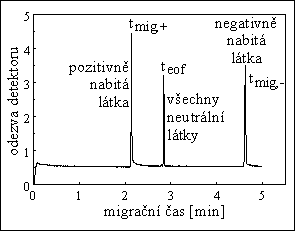
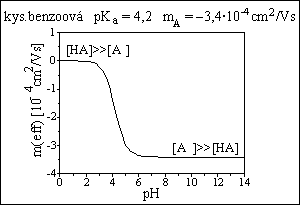
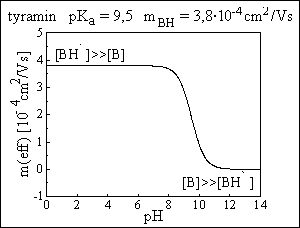
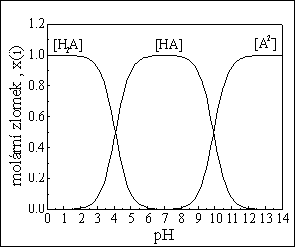
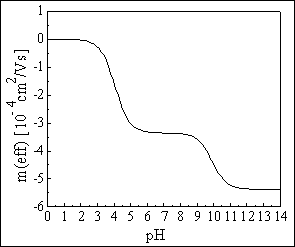
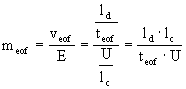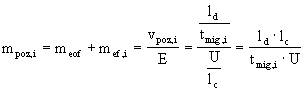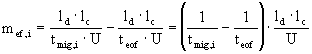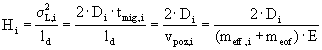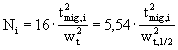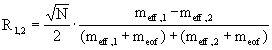kvalitativní informace :
poloha píku - migrační čas → elektroforetická pohyblivost - druh látky
(metoda standardů)
kvantitativní informace :
plocha píku → množství, koncentrace látky
a) metoda kalibrační přímky
b) metoda standardního přídavku
c) metoda vnitřního standardu
CZE ANORGANICKÝCH ANIONTÙ
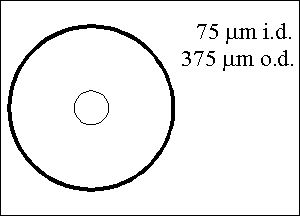
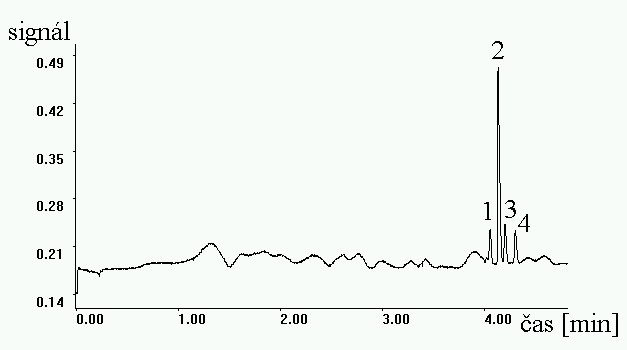
kapilára : 75 μm i.d., 61 cm, 72 cm
separační pufr : 5 mM K2CrO4 + 0,5 mM TTAB (pH = 8,0)
separační napětí : -15 kV (15 μA)
dávkování vzorku : 20 mBar / 6 s (≈ 13 nl)
nepřímá fotometrická detekce při 254 nm
píky :
1. chloridy (18 mg/l; 0,2 ng ve 13 nl)
2. sírany (69 mg/l; 0,9 ng ve 13 nl)
3. dusitany (20 mg/l; 0,3 ng ve 13 nl)
4. dusičnany (19 mg/l; 0,2 ng ve 13 nl)
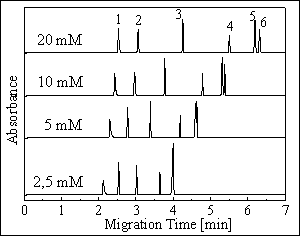
CZE ANORGANICKÝCH KATIONTÙ
kapilára : 75 μm i.d., 51 cm, 51 cm
separační pufr : 20 mM kyselina citronová + 10 mM LiOH (pH = 2,8)
separační napětí : 30 kV (13 μA)
dávkování vzorku : 10 mBar / 6 s (≈ 9 nl)
vodivostní detekce
píky :
1. K+ (195 mg/l; 2 ng v 9 nl)
2. Na+ (115 mg/l; 1 ng v 9 nl)
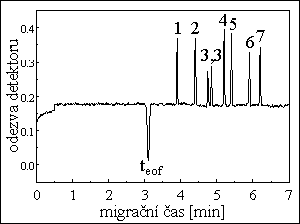
CZE HERBICIDÙ
kapilára : 50 μm i.d., 40 cm, 47 cm
separační pufr : 20 mM fosforečnan (pH = 5,6) + 2 mM α-cyclodextrin
separační napětí : 25 kV
dávkování vzorku : 35 mBar / 4 s (≈ 4,5 nl)
přímá UV fotometrická detekce při 200 nm
píky :
1. 4-(2,4-dichlorfenoxy)máselná kyselina
2. 4-(4-chlor-2-metylfenoxy)máselná kyselina
3. 2-(2,4-dichlorfenoxy)propionová kyselina
4. 2,4-dichlorfenoxyoctová kyselina
5. 4-chlor-2-metylfenoxyoctová kyselina
6. 2-(2,4,5-trichlorfenoxy)propionova kyselina
7. 2,4,5-trichlorfenoxyoctová kyselina
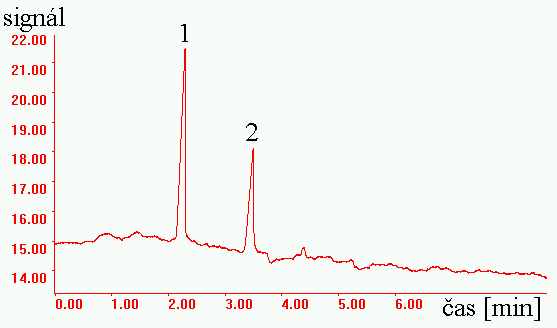
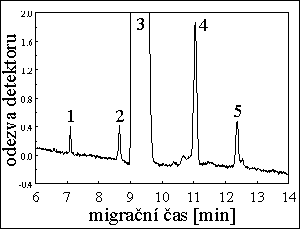
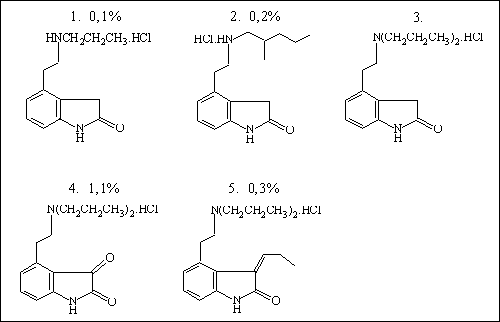
CZE ROPINIROLU A JEHO NEČISTOT
kapilára : 50 μm i.d., 40 cm, 47 cm
separační pufr : 100 mM Na2B4O7 + 30 mM MgSO4 (pH = 8,7) s 20% CH3CN
separační napětí : 30 kV (33 μA)
dávkování vzorku : 11 nl ( 2 mg/ml )
přímá UV fotometrická detekce při 254 nm
soubory pdf: preSM5.pdf preSM6.pdf czeA.pdf czeB.pdf
[ Domovská stránka |
Separační metody |
HPLC |
GC |
CES |
CZE |
MECC |
CEC |
TLC a PC |
Extrakce, GPC, IEC a AC |
Otázky |
Cvičení |
Témata |
Kvalitativní analytická chemie |
Základní praktika |
Seminář z analytické chemie |
Analytické separační metody ]
Analytické separační metody ]
24.1.1996 © Pavel Coufal