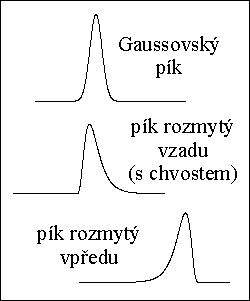
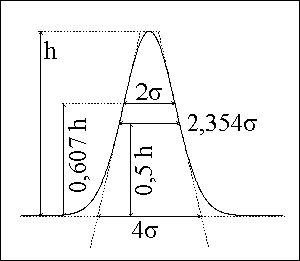
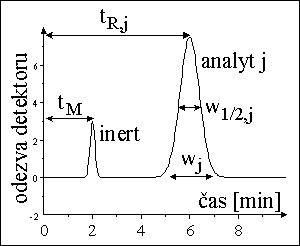
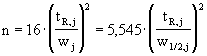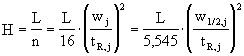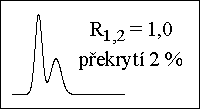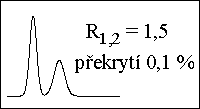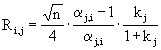kvalitativní informace :
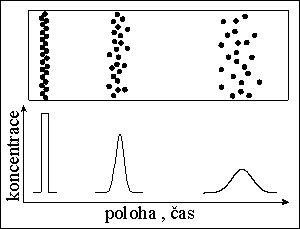
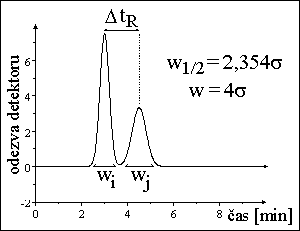
poloha píku - retenčnķ čas → retenčnķ faktor, distribučnķ konstanta - druh látky
(metoda standardů)
kvantitativní informace :
plocha píku → množstvķ, koncentrace lįtky
a) metoda kalibračnķ přķmky
b) metoda vnitřnķho standardu
c) metoda standardnķho přķdavku
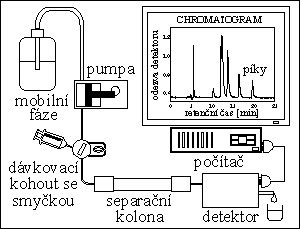
PUMPY
tlak mobilnķ fįze až do 40 MPa
čerpadla nebo lineįrnķ dįvkovače
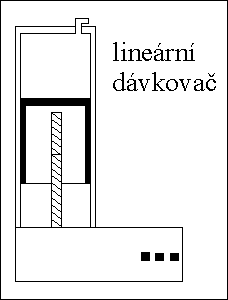
DÁVKOVACÍ KOHOUTY
majķ dįvkovacķ smyčku (dįvkujķ se desķtky μl)
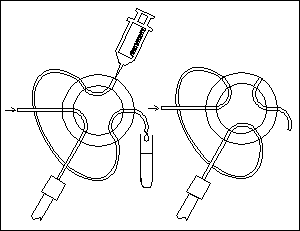
KOLONY
Rovné skleněné trubice o délce 10 až 25 cm a vnitřnķm průměru
3 , 4 nebo 4,6 mm naplněné sorbentem o průměru zrn 3 , 5 nebo 10 μm,
kterż je držen v kolně pomocķ frit.
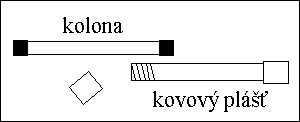
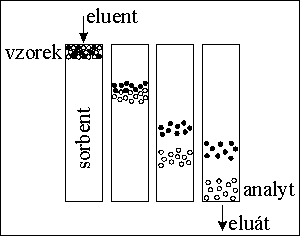
STACIONÁRNÍ FÁZE pro LSC
silikagel (oxid křemičitż) - polįrnķ, kyselż
alumina (oxid hlinitý) - polární, bazický
aktivní uhlí - téměř nepolįrnķ, jen zřķdka
MOBILNÍ FÁZE pro LSC
elučnķ sķla roste → pentan, benzen, chloroform, aceton, acetonitril, ethanol, methanol, voda
STACIONÁRNÍ FÁZE pro LLC
a) stacionární fáze mechanicky nanesené na inertnķm nosiči
(ethylenglycol nebo skvalan na silikagelu)
b) stacionární fáze chemicky vázané (zakotvené) na inertnķm nosiči (tj. silikagelu)
≡Si-C18H37 -C8H17 -(CH2)3C6H5 nepolární
-(CH2)3-CN -(CH2)3-NH2 -O-(CH2)2-OH polární
MOBILNÍ FÁZE pro LLC
a) chromatografie s normálními fázemi (stac. fáze polární a mob. fáze nepolární)
pentan, heptan, chloroform a jejich směsi
b) chromatografie s obrácenými (reverzními) fázemi (RP-HPLC)
(stac. fáze nepolární a mob. fáze polární)
methanol, acetonitril, tetrahydrofuran, voda a jejich směsi
isokratická a gradientová eluce
STACIONÁRNÍ FÁZE pro IEC
měniče iontů s nabitżmi funkčnķmi skupinami
~COO- ~SO3- ~NH3+
~CH2N+(CH3)3
~SO3-H+ + Na+ ↔ ~SO3-Na+ + H+
~NH3+OH- + NO3- ↔ ~NH3+NO3- + OH-
MOBILNÍ FÁZE pro IEC
roztoky anorganických kyselin a zásad o dané iontové síle a daném pH
STACIONÁRNÍ FÁZE pro GPC, GF, SEC
polystyren zesķťovanż divinylbenzenem a silikagel o určité velikosti pórů
MOBILNÍ FÁZE pro GPC, GF, SEC
vodné pufry (např. fosforečnanovż, TRIS), acetonitril a kys. trifluoroctová (TFA)
DETEKTORY
1) absorpčnķ fotometrickż detektor
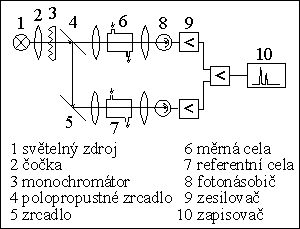
2) fluorimetrickż detektor (fluorescenčnķ det.)
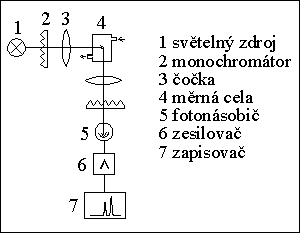
3) refraktometrický detektor
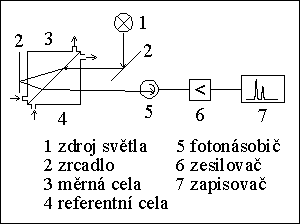
4) amperometrický detektor
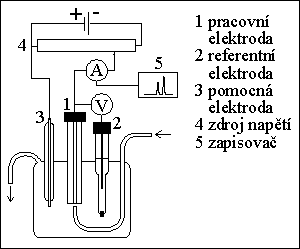
5) vodivostní detektor
6) detektor s diodovým polem (DAD)
7) hmotnostní spektrometr jako detektor
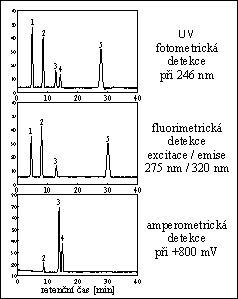
HPLC FUNGICIDÙ
extrahovaných dichlormetanem z ovoce
stac. fáze : Nucleosil 7 C18
eluent : 5 g/l kys. mravenčķ + NaOH (pH 7,5) 40 % se 60 % methanolu
píky : 1. thiabendazol, 2. o-fenylfenol, 3. difenylamin, 4. ethoxychin, 5. bifenyl
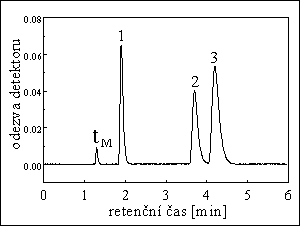
HPLC DERIVÁTÙ PURINU
kolona : 30 cm x 4 mm
stac. fáze : Nucleosil 50-5
eluent : methanol / voda / dichlormethan 47 / 17 / 936 (v/v/v)
průtok eluentu : 0,8 ml/min při tlaku 100 bar
detekce : UV fotometrickį při 280 nm
píky : 1. kofein, 2. theofyllin , 3. theobromin
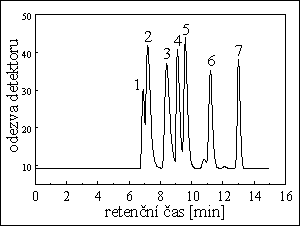
HPLC BÍLKOVIN
kolona : 25 cm x 9,4 mm
stac. fáze : Zorbax GF-250
eluent : 130 mM NaCl + 20 mM KCl + 50 mM Na2HPO4 (pH = 7,0)
průtok eluentu : 1 ml/min
detekce : UV fotometrickį při 210 nm
píky :
1. myí IgM, Mh = 900 000
2. hovězķ thyroglobulin, Mh = 669 000
3. β-amylasa z brambor, Mh = 200 000
4. hovězķ serum albumin, Mh = 66 000
5. kuřecķ albumin, Mh = 45 500
6. hovězķ RNAasa, Mh = 13 700
7. azid (tmax), Mh = 65
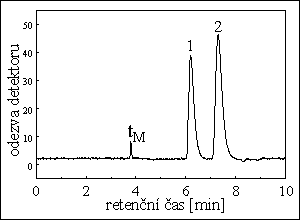
HPLC D,L ALANINU
chirįlnķ separace optickżch izomerů
kolona : 25 cm x 4 mm
stac. fáze : Nucleosil Chiral-1
eluent : 1 mM vodný roztok (CH3COO)2Cu (pH = 5,6)
průtok eluentu : 1,2 ml/min při tlaku 75 bar
teplota : 60 ˚C
detekce : UV fotometrickį při 240 nm
píky : 1. D-alanin, 2. L-alanin
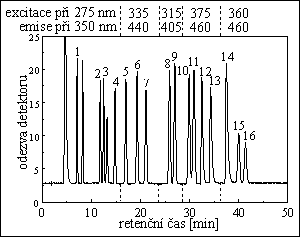
POLYAROMATICKÉ UHLOVODÍKY
kolona : 15 cm x 4 mm
stac. fáze : Nucleosil 5 C18 PAH
průtok eluentu : 0,9 ml/min při tlaku 100 bar
eluent : acetonitril / voda
5 min 60% ACN, isokraticky
60% → 90% ACN za 15 min, lineární gradient
90% → 100% ACN za 20 min, lineární gradient
20 min 100% ACN, isokraticky
detekce : fluorimetrická
píky : 1. naftalen, 2. acenaften, 3. fluoren, 4. fenanthren, 5. anthracen, 6. fluoranthen, 7. pyren,
8. benz[a]antracen, 9. chrysen, 10. benzo[e]pyren, 11. benzo[b]fluoranthen,
12. benzo[k]fluoranthen, 13. benzo[a]pyren, 14. dibenzo[ah]anthracen, 15. benzo[ghi]perylen,
16. indeno[1,2,3-cd]pyren
soubory pdf: preSM2.pdf preSM3.pdf hplcA.pdf hplcB.pdf hplcC.pdf
[ Domovskį strįnka |
Separačnķ metody |
HPLC |
GC |
CES |
CZE |
MECC |
CEC |
TLC a PC |
Extrakce, GPC, IEC a AC |
Otįzky |
Cvičenķ |
Témata |
Kvalitativnķ analytickį chemie |
Zįkladnķ praktika |
Seminįų z analytické chemie |
Analytické separačnķ metody ]
2.3.1996 © Pavel Coufal