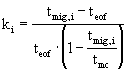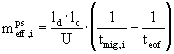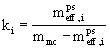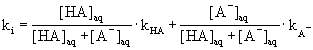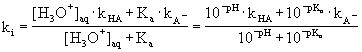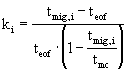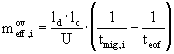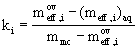ELUČNÕ OKNO v MECC a HPLC
MECC
HPLC
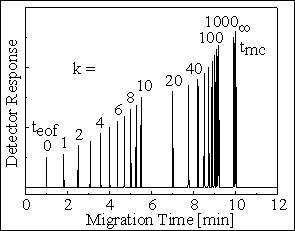
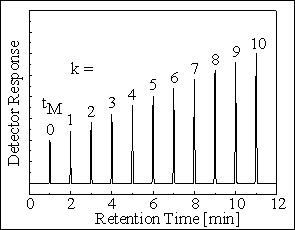
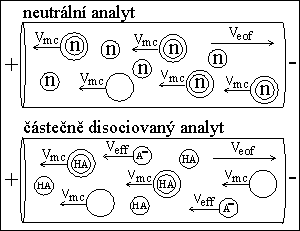
DISTRIBUCE NEUTRÁLNÍCH LÁTEK v MECC
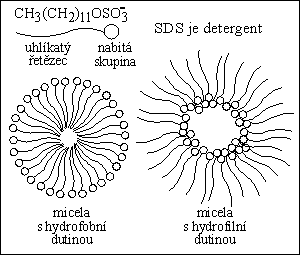
micelární fáze = pseudostacionární fáze = mc
vodná fáze = aq
distribučnÌ konstanta :
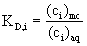
retenčnÌ faktor :
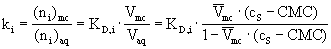
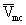 parciální molární objem micel
parciální molární objem micel
pro malé koncentrace detergentu :
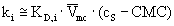
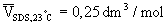
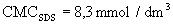
POZOROVANÁ RYCHLOST NEUTRÁLNÍCH LÁTEK v MECC
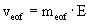
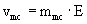
mmc efektivní mobilita micel
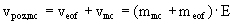
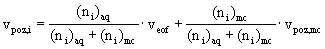
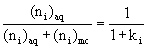
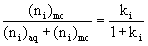
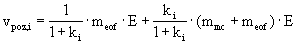
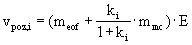
z elektroferogramu : teof , tmig,i , tmc
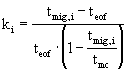
PSEUDOEFEKTIVNÍ MOBILITA NEUTRÁLNÍCH LÁTEK v MECC
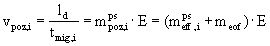
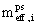 pseudo-efektivní mobilita
pseudo-efektivní mobilita
z elektroferogramu : tmig,i , teof
(nepotřebujeme zn·t tmc)
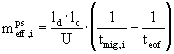
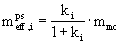
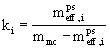
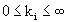

DISTRIBUCE NABITÝCH LÁTEK v MECC
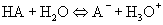
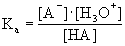
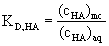
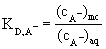
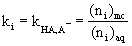
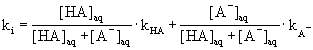
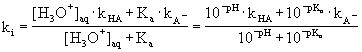
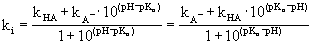
z elektroferogramu : nelze použÌt n·sledujÌcÌ rovnici
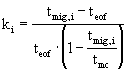
CELKOVÁ MOBILITA NABITÝCH LÁTEK v MECC
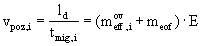
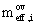 celková (overall) efektivní mobilita
celková (overall) efektivní mobilita
z elektroferogramu : tmig,i , teof
(nepotřebujeme zn·t tmc)
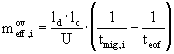
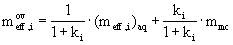
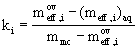
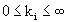
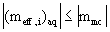 pak
pak 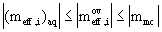
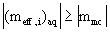 pak
pak 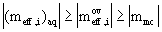
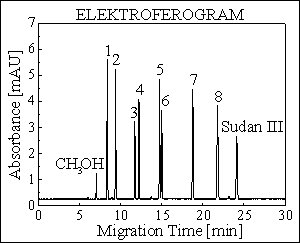
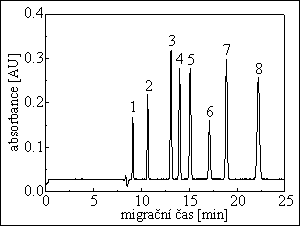
MECC : VITAMÍNY
100 μm I.D., 50 cm, 80 cm
20 mM Na2HPO4 / Na3PO4 (pH = 9,0), 50 mM SDS
15 kV (100 μA)
UV detekce při 254 nm
píky :
1 nikotinamid (B3), 2 pyridoxin (B6), 3 kyanokobalamin (B12), 4 kyselina askorbová (C),
5 riboflavin (B2), 6 kyselina nikotinová, 7 ethyl-p-aminobenzo·t (vnitřnÌ standard), 8 thiamin (B1)
MECC : TONIC
75 μm I.D., 61 cm, 72 cm
25 mM Na2B4O7 (pH = 9,2), 25 mM SDS
20 mbar / 0,10 min (≈ 13 nl)
20 kV (76 μA)
UV detekce při 254 nm
píky :
1 kyselina askorbová (68 mg/l; 0,9 ng ve 13 nl)
2 kyselina sorbová (174 mg/l; 2,3 ng ve 13 nl)
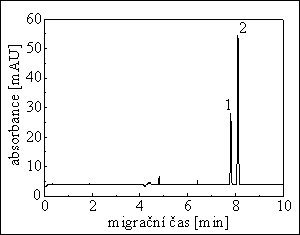
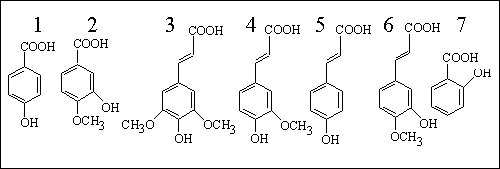
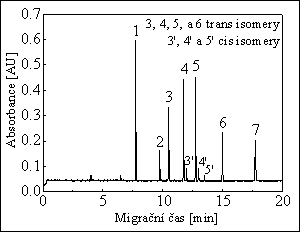
MECC : karboxylové kyseliny
50 μm I.D., 44,5 cm, 65,7 cm
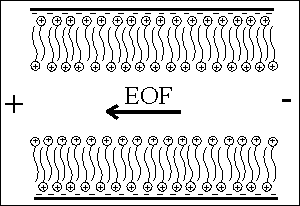
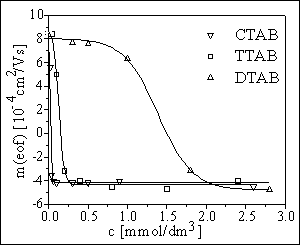
18 mM Na2B4O7 + 30 mM NaH2PO4 + 50 mM CTAB
Separace : -20 kV
Detekce : UV při 280 nm
soubor pdf: mecc.pdf
[ Domovsk· str·nka |
SeparaËnÌ metody |
HPLC |
GC |
CES |
CZE |
MECC |
CEC |
TLC a PC |
Extrakce, GPC, IEC a AC |
Ot·zky |
CviËenÌ |
TÈmata |
KvalitativnÌ analytick· chemie |
Z·kladnÌ praktika |
Semin·¯ z analytickÈ chemie |
AnalytickÈ separaËnÌ metody ]
28.1.1996 © Pavel Coufal